КАРАЧИ, грязевой курорт в Новосибирской обл. РСФСР. Расположен в сев.
части Барабинской низм., в 394 км от Новосибирска. Лето тёплое (ср.
темп-ра июля 19 0C), зима холодная (ср. темп-ра янв. -19 0C);
осадков 270 мм за год. Леч. средства: иловая грязь с большим содержанием
сероводорода и хлоридно-сульфатная натриево-магниевая рапа оз. Карачи;
минеральная вода с составом
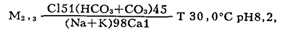
используемая для питьевого лечения. Лечение больных с заболеваниями
опорно-двигат. аппарата, периферич. нервной системы, органов пищеварения,
гинекологическими. Санаторий, поликлиника, водогрязелечебница.
КАРАШ-СЕВЕРИН (Caras-Severin), уезд на Ю.-З. Румынии, преим. в
Банатских горах. Пл. 8,5 тыс. км2. Нас. 366,3 тыс. чел.
(1970). Адм.ц. - г. Решица. Уезд даёт 2,7% валового пром. произ-ва и 1,1% валового
с.-х. произ-ва страны. Чёрная металлургия и машиностроение (Решица, Оцелу-Рошу,
Бокша), деревообр. (Карансебеш) и пищ. промышленность. Добыча железной
(Окна-де-Фьер) и медной (Молдова-Ноуэ) руд. Посевы кукурузы, пшеницы,
картофеля, льна-кудряша. В предгорьях - садоводство. Поголовье (1971, в тыс.):
кр. рог. скота 84, свиней 35, овец 269. В 40 км к С. от г. Турну-Северин
бальнеологич. курорт Бэиле - Еркулане, источниками к-рого пользовались
ещё древние римляне.
КАРАЯH (Karajan) Герберт фон (р. 5.4.1908, Зальцбург), австрийский
дирижёр. Муз. образование получил в "Моцартеуме" в Зальцбурге. В
1927-34 дирижировал в оперном театре г. Ульм, в 1934- 1941- в г. Ахен; в
1941-44 руководил Берлинской гос. капеллой. В послевоенные годы К. занимает
одно из ведущих мест в зап.-европ. муз. жизни. С 1947 дирижёр Общества друзей
музыки в Вене, участник фестивалей в Зальцбурге, Вене, Байрёйте, Берлине,
Мюнхене и др.; гастролирует с оркестрами Венской и Лондонской филармоний;
выступает как дирижёр и режиссёр во мн. европ. оперных театрах. С 1955 К.
возглавляет Берлинский филармонич. оркестр (Зап. Берлин), одновременно муз.
руководитель Венской гос. оперы (1956-64) и Зальцбургских фестивалей (1957-60).
В 1962, 1964 и 1969 выступал в СССР. Для исполнит, искусства К. характерно
точное воспроизведение авторского текста, безукоризненное чувство музыкальной
формы, яркое проявление волевого начала.
Лит.: Рубин M., Три портрета, "Советская музыка", 1962, №
4; H е г z f e l d F., Herbert von Karajan, 2 Aufl., В., 1962.
E. Я. Рацер.
КАРБАЗОЛ, дибензопиррол, гетероциклическое соединение; бесцветные
кристаллы, не растворимые в воде, растворимые в органич. растворителях; tпл
245- 247 0C, tкип 354-355 0C; слабое
основание, образующее нестойкие соли с кислотами. К. выделяют из кам.-уг. смолы
(из антраценового масла), а также получают синтетически из аминодифенила,
фенантрена и др. К. применяют в произ-ве красителей, лекарственных веществ и
инсектицидов.
КАРБАМИД, амид угольной кислоты (NH2)2CO, то
же, что мочевина.
КАРБАМИДНЫЕ ПЛАСТИКИ, то же, что аминопласты.
КАРБАМЙДНЫЕ СМОЛЫ, продукты поликонденсации формальдегида с мочевиной
(карбамидом) и её производными: тиомочевиной, дициакдиамидом, меламином и др.
Из карбамидных смол технич. значение для произ-ва термореактивных пластмасс и
клеёв получили гл. обр. мочевино-формальдегидные смолы и меламино-формальдегидные
смолы.
КАРБАМИДНЫЙ КЛЕЙ, клей на основе мочевино-формальдегидных смол и
меламино-формальдегидных смол (т. н. карбамидных смол), а также их
смесей. К. к. в больших количествах применяют в деревообрабат. пром-сти, гл.
обр. при изготовлении фанеры, мебели и др.; используют для склеивания фарфора и
металла.
К. к. представляет собой водный раствор карбамидной смолы. Часто в состав
клея входит отвердитель (щавелевая, фталевая, соляная кислоты или нек-рые
соли) и наполнитель (мука бобовых или злаков, крахмал, древесная мука, гипс и
т. п.). Напр., клей К-17 состоит из 100 частей (по массе) смолы МФ-17, 7- 22
частей 10% -ного водного раствора щавелевой кислоты и 6-8 частей древесной
муки.
К. к. готовят путём смешения раствора смолы с другими ингредиентами клея
(если они входят в состав композиции). Иногда клей готовят в виде вспененной
массы. Жизнеспособность К. к. в зависимости от типа клея колеблется от 0,5 до
48 ч. Срок хранения К. к. без отвердителя в значит, мере зависит от темп-ры;
так, клей ММФ можно хранить 12 мес. при 10 0C и только 0,5 мес.
при 40 0C. Введение в клей аммиачной воды, уротропина, мочевины
или меламина позволяет увеличить срок хранения К. к. в 2 раза.
К. к. может отверждаться как при нагревании, так и при нормальной темп-ре
(только в присутствии отвердителя). Подготовка склеиваемой поверхности при
использовании К. к. не отличается от общепринятой. Обычно К. к. наносят кистью,
а низковязкие композиции - распылением, дают им подсохнуть (иногда эта стадия
исключается), а затем склеиваемые детали соединяют под давлением 0,15-1,7 Мн/м2
(1,5-17 кгс/см2). При использовании К. к. горячего
отверждения склеиваемые детали в прессе подвергают нагреву. К. к. образуют
клеевые соединения, обладающие хорошей механич. прочностью [10-13 Мн/м2
(100- 130 кгс/см2)] и удовлетворит, стойкостью
к действию влаги. К. к. на основе меламино-формальдегидных смол обладают
лучшими качествами, чем клеи на основе мочевино-формальдегидных смол, однако
последние значительно дешевле. Поэтому часто практикуют смешение
мочевино-формальдегидной смолы с небольшим количеством меламино-формальдегидной
смолы, что значительно улучшает качество клея.
Лит. см. при ст. Клеи.
КАРБАНИОНЫ, молекулярные частицы, содержащие отрицательно заряженный
трёхковалентный атом углерода
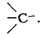
К. чрезвычайно реакционноспособны и поэтому малоустойчивы; являются
промежуточными частицами во многих органич. реакциях (ср. Карбония ионы). К.
образуются, напр., при действии сильных оснований В: (точки означают
неподелённую электронную пару) на углеводороды, от к-рых какой-либо из атомов
водорода легко уходит в виде протона:
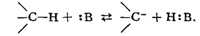
Так, при действии амида натрия на три-фенилметан образуется
трифенилметил-натрий - ионно построенное ярко-красное соединение, содержащее
трифенил-метильный анион: (C6H5)3CH+Na+NH2-->(C6H5)3C-Na++NH3
Этот К. устойчив вследствие распределения отрицательного заряда между
несколькими атомами углерода.
Большинство металлоорганич. соединений построено ковалентно, однако из-за
поляризации связи металл - углерод появляется избыточная электронная плотность
у атома углерода, связанного с металлом; такой атом имеет частичный
карбанионный характер. Поэтому в реакциях металлоорганич. соединения служат
донорами К.
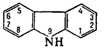
Особым видом К. являются илиды - биполярные ионы, содержащие положительно
заряженный гетероатом (N, P, As, О, S) и отрицательно заряженный атом углерода,
как, например, флуоренилилид пиридиния:
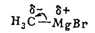
Существование К. в виде кинетически независимых частиц строго доказано в
немногих случаях, однако представление об их промежуточном образовании часто
привлекается для трактовки механизма орга-нич. реакций, многие из к-рых имеют
большое теоретич. и прикладное значение (напр., анионная полимеризация).
Лит.: Крам Д., Основы химии карбанионов, пер. с англ., M., 1967; Б р
е с л о у Р., Механизмы органических реакций, пер. с англ., M., 1968.
В. Л.
Дяткин.
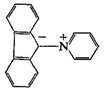
КАРБГЕМОГЛОБИН, HbCO2, соединение гемоглобина (Hb)
с углекислым газом (CO2); связь между ними легко образуется, но и
легко распадается. Выделяющийся в процессе жизнедеятельности тканей CO2
диффундирует в капилляры, где частично вступает в связь с Hb (отдавшим до того
свой кислород тканям). В лёгких CO2 отщепляется от К., содержащегося
в эритроцитах. В форме К. транспортируется около трети CO2,
выделяемого через лёгкие (большая часть CO2 транспортируется в
форме солей угольной к-ты, содержащихся в плазме и эритроцитах).
КАРБЕНЫ, неустойчивые органич. соединения, содержащие
электронейтральный двухвалентный атом углерода R'R"C: (точки означают два
электрона); промежуточные частицы во многих органич. реакциях. Так, простейший
К.- метилен : CH2 образуется при термич. или фотохимич. разложении
диазомета-на или кетена, напр.:
CH2N2->
:CH2-HN2.
Аналогично могут быть получены и др. К. Дигалогенкарбены возникают при
термич. разложении щелочных солей три-галогенуксусных K-T:
CCl3COONa ->
:CCl2+NaCl+CO2.
К. стабилизируются различными путями в зависимости от условий генерации и природы
взаимодействующих с ними соединений. Напр., они могут димеризоваться: : CH2
+ :СН2 -> CH2 = CH2; внедряться по связи
углерод - водород, напр, в углеводороды: R - H + :СН2 -> -> R
- CH3; присоединяться по кратной связи (напр., к этилену) с
образованием трёхчленного цикла:
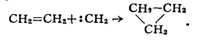
Последнюю реакцию широко применяют для синтеза различных трёхчленных циклич.
соединений.
Лит.: Кнунянц И. Л., Гамбарян H. П., Poхлин E. M., Карбены,
"Успехи химии", 1958, т. 27, в. 12, с. 1361.
Б. Л. Дяткин.
КАРБИД БОРА, см. Бора карбид.
КАРБИД КАЛЬЦИЯ, CaC2, соединение кальция с углеродом; один
из важнейших карбидов, применяемых в технике. Химически чистый К. к.
бесцветен (технический - от светло-бурого до чёрного); плотн. 2,2 г/см3,
tпл 2300 0C. С водой взаимодействует с образованием
ацетилена: CaC2 + 2H2O = C2H2 +
Ca(OH)2; для отвода выделяющейся теплоты (30,4 ккал/молъ, т.
е. 127,3 кдж/моль) процесс ведут в избытке воды. К. к. при нагревании
взаимодействует с азотом, образуя цианамид кальция:
CaC2 + N2
= Ca(CN)2,
Получают К. к. в электрич. печах при 1900-1950° С по реакции: CaO + 3C = =
CaC2 + СО, в к-рой поглощается большое количество тепла (450,5 кдж/моль).
Сырьём служат известь и антрацит или кокс. Большинство действующих
карбидных печей открыто сверху; СО по выходе из печи сгорает до CO2.
Разработаны также конструкции закрытых печей с отбором СО. К. к. широко
применяют в технике, главным образом для произ-ва ацетилена, цианамида кальция
и восстановления щелочных металлов.
Лит.: Кузнецов Л. А., Производство карбида кальция, M.- Л., 1950; Стрижевский И. И., Гузов С. Г. и Ковальский В. А., Ацетиленовые станции, 2
изд., M., 1959.
КАРБИД КРЕМНИЯ, карборунд, SiC, соединение кремния с углеродом; см. Кремния
карбид.
КАРБИДКРЕМНИЕВЫЕ ОГНЕУПОРHЫE ИЗДЕЛИЯ, изготовляются из карбида
кремния (карборунда) с добавками и содержат от 20-35 до 70-98% SiC. К. о. и.
различаются по способу связывания зёрен карбида кремния: на кремнезёмистой
(образующейся при окислении карбида), нитридной (SiaNO, оксинитридной (Si2ON2),
алюмосиликатной связках, а также рекристаллизованные, самосвязанные и др.
Изделия формуют на прессах или другим способом из порошкообразных смесей,
содержащих карбид кремния, и обжигают при 1300-1550 0C (нек-рые виды
- при 2000-2200 0C). Характерные свойства К. о. и.: высокая
теплопроводность [7-17 вт/(к-К) при 800 0C] и связанная с этим
хорошая термостойкость; устойчивость против деформации при высоких
темп-pax. При 1300-1500 °С в окислит, среде К. о. и. постепенно окисляются,
особенно при избытке кислорода и в присутствии водяного пара. К. о. и.
применяются, напр., в рекуператорах, муфельных печах, агрегатах цветной
металлургии, этажерках туннельных вагонеток при обжиге фарфора и керамики,
котельных топках.
Лит.: К а й н а р с к и й И. С., Д е г т я
р ё в а Э. В.,
Карборундовые огнеупоры, Хар., 1963.
А. К. Карклит.
КАРБИДЫ, соединения углерода с электроположительными элементами, гл. обр.
с металлами и нек-рыми неметаллами По типу хим. связи К. могут быть
подразделены на три основные группы: ионные (или солеобразные), ковалентные и
ме-таллоподобные. Нек-рые К. принадлежат к нестехиометрическим соединениям -
твёрдым веществам переменного состава, не отвечающего стехиометрич.
законам.
Ионные К. образуются сильно электроположительными металлами; они содержат
катионы металлов и анионы углерода. К ним относятся ацетилениды с анионами [С =
C]2-, к-рые могут быть представлены как продукты замещения
водорода в ацетилене C2H2 металлами, а также метаниды -
продукты замещения металлами водорода в метане СН4.
Табл. 1. - Свойства некоторых ионных карбидов
|
|
Кристаллическая структура
|
|
|
Теплота образования, ккал/моль *
|
Уд. объёмное электрич. сопротивление,
MKOM • CM
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
*1 ккал/моль =4,19 кдж/моль.
Ацетиленидами являются К. щелочных металлов (Li2Ca, Na2C2
и пр.), магния MgC2 и щелочноземельных металлов (CaC2,
SrC2 и др.), высшие К. редкоземельных металлов (YC2, LaC2
и др.) и актиноидов (ThC2 и пр.). С уменьшением ионизационного потенциала
металла в этой группе возрастает склонность к образованию
"поликарбидов" со сложными анионами из атомов углерода (MeCs, MeCie,
MeC24 и др.). Эти К. имеют графитоподобные решётки, в к-рых между
слоями из атомов углерода расположены атомы металла. Ионные К. ацетиленидного
типа, напр, карбид кальция, при взаимодействии с водой или разбавл.
к-тами разлагаются с выделением ацетилена (или ацетилена в смеси с др.
углеводородами и иногда - водородом). Cu2C2, Ag2C2
и др. взрываются при ударе, обладают невысокой хим. устойчивостью, легко
разлагаются и окисляются при нагревании. К метанидам относятся Be2C,
AL4C3, к-рые легко гидролизуются с выделением метана
(табл. 1).
Ковалентные К., типичными представителями к-рых являются К. кремния и бора,
SiC и B.sC (правильнее B12C3), отличаются прочностью
межатомной связи; обладают высокой твёрдостью, хим. инертностью,
жаропрочностью; являются полупроводниками. Структура нек-рых таких К. (напр.,
SiC) близка к структуре алмаза. Кристаллич. решётки этих К. представляют
собой гигантские молекулы (см. Бора карбид, Кремния карбид).
Металлоподобные К. обычно построены как фазы внедрения атомов углерода в
поры кристаллических решёток переходных металлов. Природа металлоподобных К.,
как фаз внедрения, обусловливает их высокую твёрдость и износостойкость,
практическое отсутствие пластичности при обычных темп-рах, хрупкость и
относительно невысокие прочие механич. свойства. К. этой группы - хорошие
проводники электричества, откуда и название -"Металлоподобные". Многие
из них - сверхпроводники (напр., темп-ры перехода в сверхпроводящее состояние
составляют: Nb2C, 9,18 К; NbC, 8-10 К; MO2C, 12,2 К; MoC,
6,5 К). Важными для техники свойствами обладают взаимные сплавы К. TiC, ZrC,
HfC, NbC и TaC. Так, композиции, состоящие из 25% HfC и 75% TaC,
Табл. 3.- Механические свойства карбидов
|
|
Твёрдость Н,Гн/мг, при температуре 0C
|
Предел прочности при растяжении, Mн/м2, при
температуре 0C
|
Предел прочности при сжатии, Мн/м2, при
температуре 0C
|
Модуль упругости, Гн/м2, при температуре
0C
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
имеют наиболее высокую темп-ру плавления (ок. 4000 0C) из всех
тугоплавких металлов и веществ. Металлоподобные К. обладают большой хим.
устойчивостью в кислотах, меньшей - в щелочах. При их взаимодействии с H2,
O2, N2 и пр.образуются гидридокарбиды,
оксикарбиды, карбонитриды, также представляющие фазы внедрения и обладающие свойствами,
близкими к свойствам К. К металло-подобным К. относятся также соединения с
более сложными структурами: Mn3C, Fe3C, Co3C,
Ni3C (табл. 2).
Получение и применение. Распространёнными методами получения К. являются нагревание
смесей порошков металлов и угля в среде инертного газа или восстановит, газа;
сплавление металлов с одноврем. карбидизацией (MeO + С -> MeC + СО) при
темп-рах 1500-2000° С и др. Для получения изделий из порошков К. используют порошковую
металлургию; отливку расплавленных К. (обычно под давлением газовой среды
для предотвращения разложения при высоких темп-pax); диффузионное
науглероживание предварительно подготовленных изделий из металлов и неметаллов;
осаждение в результате реакций в газовой фазе (особенно при получении карбидных
волокон); плазменную металлургию. Обычные механич. методы обработки изделий из
металлоподобных К. и высокопрочных карбидно-металлич. сплавов оказываются
непригодными и заменяются абразивной, ультразвуковой обработкой, электроискровым
способом и др.
Из ионных К. важное значение в технике как источник ацетилена имеет карбид
кальция. Широко используются ковалентные и металлоподобные К. Так, тугоплавкие
К. применяют для изготовления нагревателей электропечей сопротивления, защитных
чехлов для термопар, тиглей и т. д. На основе сверхтвёрдых и износостойких К.
производят металло-керамич. твёрдые сплавы (вольфрамокобальтовые и
титановольфрамовые), а также абразивы для шлифования и доводки (особенно SiC и
B4C). К. входят в состав жаропрочных и жаростойких сплавов - керметов,
в к-рых твёрдые, но хрупкие К. цементированы вязкими, но достаточно
тугоплавкими металлами. К. железа Fe3C образует в железоуглеродистых
сплавах (чугунах и сталях) т. н. цемен-титную фазу - твёрдую, но очень хрупкую
и непластичную (см. Цементит). Высокая хим. стойкость К. используется в
хим. машиностроении и хим. пром-сти для изготовления трубопроводов, насадок,
облицовки реакторов. Металлич. или полупроводниковая проводимость, хорошие термоэмиссионные
свойства, способность переходить в сверхпроводящее состояние - для изготовления
резисторов, различных элементов полупроводниковых устройств, в составе
электрокон-гактов, магнитных материалов, термокатодов в электронике.
Лит.: Самсонов Г. В., Тугоплавкие соединения. Справочник по свойствам
и применению, M., 1963; Косолапова Т. Я., Карбиды, M., 1968; Тугоплавкие
материалы в машиностроении. Справочник, под ред. А. Т. Туманова и К. И.
Портного, M., 1967; Особо тугоплавкие элементы и соединения. Справочник, M.,
1969; Тугоплавкие карбиды. [Сборник], под ред. Г. В. Самсонова, К., 1970.
Г. В. Самсонов, К. И. Портной.
КАРБИДЫ ЖЕЛЕЗА, соединения железа с углеродом; см. Железо,
Железоуглеродистые сплавы, Карбиды.
Табл. 2.- Свойства некоторых металлоподобных и ковалентных карбидов
|
|
Границы области однород- ности, ат. %С
|
Кристал-лическая струк- тура а)
|
|
Темпе- ратура плав-ления,
0C
|
Теплота образо- вания, ккал/мольд)
|
Коэфф. термиче-
ского
расши-
рения (20 -1800 0C)
(1/1 0C)
x 106
|
Теплопро-водность, кал/см сек*°Се)
|
Уд. объём- ное элек- трич. сопро- тивление, MKOM
см
|
Работа выхода электро-
нов ж) ф эфф,эв
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
о) КГЦ - кубическая гранецентрированная, Ромбич. - ромбическая,
Ромбоэдр. - ромбоэдрическая, ГПУ - гексагональная плотноупакованная, Гекс. -
гексагональная. б) Разлагается. в) 20-1000 0C.
г) % по массе. д) 1 ккал/моль = 4,19 кдж/моль. е)
1 кал/см-сек - 0C= 419 вт/(м-К). ж) При 1800 K.
КАРБИН, 4-хлор-6утин-2-ил-N-(3-хлорфенил)-карбамат, системный гербицид,
применяется для борьбы с овсюгом в посевах пшеницы, ячменя, сах. свёклы,
льна, подсолнечника, зернобобовых и крестоцветных культур.
КАРБИНОЛЫ, общее название алифатических спиртов, рассматриваемых как
производные метилового спирта - карбинола CH3 - ОН. Напр.,
изопропиловый спирт (CHs)2CHOH наз. диметил-карбинол. См. Спирты.
КАРБИНОЛЬНЫЕ ЛАКИ, лаки на основе карбинольных смол.
КАРБИНОЛЬНЫЕ СМОЛЫ, синтетические полимеры, продукты сополимеризации
диметилвинилэтинилкарбинола CH2 = CH-C = C-C(CH3)2-OH
гл. обр. с бутил- и (или) метилметакрила-том. На основе К. с. получают
карбинольные лаки и карбинольный клей.
Карбинольные лаки - бесцветные или окрашенные растворы К. с. в
этилцеллозольве и (или) этиловом спирте; сухой остаток лаков 23-45%,
продолжительность высыхания при 20 0C 30-90 мин. Бесцветные
лаки применяют для лакирования многокрасочной печатной продукции с целью
улучшения её внешнего вида, прочности и водостойкости. Окрашенные лаки
(краситель - основной синий К) используют при бескопировочном черчении для
лакиро-вания чертежей, выполненных карандашом ("люмограф",
"светокопия") на прозрачной чертёжной бумаге.
Карбинольный клей - композиция на основе К. с., содержащая наполнитель
(портландцемент) и растворитель (ацетон). Жизнеспособность клея 1-2,5 ч в
условиях хранения при 5-10 0C и отсутствии воздействия прямого
солнечного света. С помощью карбинольного клея склеивают металлы, керамику,
пластмассы при комнатной темп-ре (выдержка 20-24 ч) или при 60-70° С (6-8
ч); избыточное давление при склеивании - не менее 50 кн/м2(0,5
кгс/см2). Клеевое соединение обладает хорошей прочностью при
сдвиге.
Лит.: Дмитриев П. И., Технико-экономическая эффективность внедрения
лака синего КС-229 для защиты чертежей, "Лакокрасочные материалы и их
применение", 1967, №b 2; Кардашов Д. А., Синтетические клеи, 2 изд., M.,
1968.
КАРБИНОЛЬНЫЙ КЛЕЙ, клей на основе карбинольных смол.
КАРБО..., КАРБОН... (от лат. carbo, род. падеж carbonis - уголь),
составная часть слов, означающая: относящийся к соединениям углерода (напр.,
карбиды, карбонаты), к углю (напр., карбонарии).
КАРБОАНГИДРАЗА, угольная ангидраза, карбонат-гидролиаза, фермент
класса лиаз, катализирующий обратимое образование угольной к-ты из
двуокиси углерода и воды: CO2 + + H2O <-> Н2СО3.
К.- металлопротеид, содержащий Zn; мол. масса ок. 30 000. Содержится в
эритроцитах, клетках почек, слизистой желудка, сетчатке глаза и др. К.
эритроцитов обеспечивает в тканях связывание CO2 кровью и быстрое
освобождение последней от CO2 в лёгких или жабрах. В почке К.
обеспечивает образование кислой мочи, в слизистой желудка - HCl, в
поджелудочной железе - бикарбонатов поджелудочного сока, в яйцеводах птиц -
образование скорлупы яиц, содержащей СаСО3, и т. д. К. специфически
и сильно угнетается сульфонамидами, содержащими ароматич. группу. К особенно
активным UH-гибиторам К. относятся диамокс (ацетазоламид), пентазан
(метазоламин) и др. средства, применяемые в борьбе с глаукомой, при
лечении заболеваний почек и нервной системы. К. обнаружена также в листьях
нек-рых растений.
E. Ю. Ченыкаева.
КАРБОКСИГЕМОГЛОБИН, HbCO, продукт присоединения СО
(углерода окись, угарный газ) к гемоглобину (Hb). Растворы К. ярко-красного
цвета, их спектр поглощения (см. вклейку т. 6 к стр. 208) характеризуется
максимумами при дл. волны 570 и 539 ммк. Расщепление К. на Hb и СО
происходит в 10 000 раз медленнее, чем расщепление оксигемоглобина на Hb и O2.
Поэтому при наличии во вдыхаемом воздухе СО кислород постепенно вытесняется из
гемоглобина. Уже при концентрации 0,1% СО в воздухе больше половины Hb крови
превращается в К.; в результате нарушается перенос O2 от лёгких к
тканям и развивается т. н. угарное отравление.
КАРБОКСИЛАТНЫЕ КАУЧУКИ, карбоксилсодержащие каучук и, сицтетич.
каучуки, в макромолекуле к-рых содержится небольшое число карбоксильных групп
-COOH.
К наиболее изученным К. к. относятся сополимеры бутадиена (или его смесей со
стиролом или акрилонитрилом) с 1-5% метакриловой кислоты. Осн. метод получения
К. к. - эмульсионная полимеризация. Отличит, особенность К. к.,
обусловленная присутствием карбоксильных групп,- способность к вулканизации окисями
и гидроокисями двухвалентных металлов, гл. обр. ZnO, MgO, Ca(OH)2. Частичное
взаимодействие карбоксильных групп с этими вулканизующими агентами при
изготовлении резиновых смесей или на др. стадиях технология. процесса,
предшествующих вулканизации, затрудняет переработку К. к. на оборудовании (см. Под
вулканизация) и ограничивает возможности их практич. использования.
Резины из К. к., особенно полученные с помощью систем, состоящих из окисей
металлов и серусодержащих вулканизующих агентов (напр., тиурама),
характеризуются высокими механич. свойствами и теплостойкостью. Напр.,
прочность при растяжении саженаполненных резин из бута диен-стирольных К. к.
(марка СКС-30-1) составляет ~40 Мн/м2 (~400 кгс/см2),
относит, удлинение ~800% , истираемость ~ 140 см3/(квт-ч). После
старения в течение 480 ч при 100 0C резины сохраняют ~90%
первоначальных прочности при растяжении и относит, удлинения. К. к. применяют в
производстве износостойких изделий (шинного протектора, подошвы обуви),
теплостойких клеёв и т. д. Более широко, чем твёрдые К. к., используют их
водные дисперсии (латексы), напр, для пропитки шинного корда с целью
повышения прочности его связи с резиной, а также для отделки кожи, бумаги и т.
д.
Лит. см. при ст. Каучуки синтетические.
КАРБОКСИЛИАЗЫ, группа ферментов класса лиаз; катализируют декарбокси-лирование
(отщепление CO2) кето- и аминокислот. Коферментом для К.,
декарбоксилирующих кетокислоты, служит KO-карбоксилаза; для К.,
катализирующих декарбоксилирование аминокислот, - пиридоксальфосфат (см. Пиридоксалевые
ферменты).
КАРБОКСИЛИРОВАНИЕ, непосредственное введение карбоксильной группы
-COOH в органич. соединения действием CO2. Напр., К. металлоорганич.
соединения происходит при пропускании CO2 через раствор этого
соединения; последующий гидролиз приводит к карбоновой кислоте:
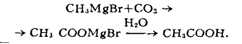
Применяемые в медицине салициловую и n-аминосалициловую к-ты (ПАСК)
получают своеобразным К. соответствующих фенолятов, напр.:
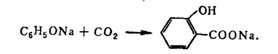
В организме К. происходит под действием специфич. ферментов; напр.,
пиру-ваткарбоксилаза катализирует К. пиро-виноградной к-ты. К. играет существ,
роль в окислении промежуточных продуктов расщепления углеводов, жиров и белков
в организме (см. Обмен веществ).
КАРБОКСИЛЬНАЯ ГРУППА, карбоксил, функциональная одновалентная
группировка
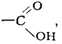
входящая в состав карбоновых кислот и определяющая их кислотные
свойства.
КАРБОКСИМЕТИЛЦЕЛЛЮЛОЗА, простой эфир целлюлозы о5щей формулы
[C6H7O2(OH)3-X (OCH2COOH)x]n.
Наибольшее практич. значение имеет натриевая соль К. (Na-K.), к-рля, как и К.,
представляет собой белое твёрдое вещество с насыпной массой 400-800 кг/м3;
плотность соли 1,59 г/см3. Растворимость Na-K. в щелочах
или в воде определяется степенью этерификации целлюлозы и условиями
растворения. Получают К. взаимодействием целлюлозы с моно-хлоруксусной кислотой
или (в производстве Na-K.) с её натриевой солью в присутствии NaOH.
Na-K. применяют для стабилизации глинистых суспензий, используемых при
бурении нефт. и газовых скважин; как добавку к моющим веществам, препятствующую
ресорбции загрязнений из моечного раствора на ткани; для шлихтования нитей
основы и как загуститель печатных красок; в качестве флотореагентов; для
повышения пластичности керамич. массы и прочности изделия-"сырца";
для регулирования реологич. свойств цем. суспензий.
Лит.: Химия и технология производных целлюлозы, под ред. Л. П.
Перепечки::а и Ю. Л. Погосова, Владимир, 1968.
КАРБОКСИПЕПТИДАЗЫ, группа ферментов из класса гидролаз (К.-А,
К.-В, К. дрожжей), катализирующих ступенчатый гидролиз полипептидов с
С-конца, т. е. с аминокислоты, у к-рой свободна карбоксильная группа
(-COOH). Мол. масса К. св. 34 000. К.-А наиболее активна в отношении ароматич.
аминокислот, К.-В - в отношении лизина или аргинина, К. дрожжей - в отношении
глицина или лизина. К. обладают также эстеразной активностью, т. е.
способностью расщеплять эфирные связи. В двенадцатиперстную кишку К.-А
поступает из поджелудочной железы, где вырабатывается в виде неактивной прокарбоксипептидазы А, превращающейся в К.-А гл. обр. под действием трипсина.
Лит.: Диксон М.,Уэбб Э., Ферменты, пер. с англ., M., 1966; Мосолов В.
В., Протеолитические ферменты, M., 1971.
КАРБОЛЕН, лекарственный препарат, таблетки активного угля.
КАРБОЛИТ, один из видов синтетич. феноло-альдегидных смол, получаемый
поликонденсацяей фенола (крезолов) с формальдегидом в присутствии нефтяных
сульфокислот (т. н. контакта Г. С. Петрова). Отечеств. пром-сть
выпускает К. с 1914.
КАРБОЛОВАЯ КИСЛОТА, C6H5OH, то же, что фенол;
применяется в медицине как антисептич. и дезикфекц. средство.
КАРБОН (от лат. carbo, род. падеж carbonis - уголь), то же, что каменноугольная
система (период).
КАРБОНАДО (исп. carbonado, от лат. carbo - уголь), разновидность алмаза,
представляющая мелкозернистые, иногда пористые агрегаты тёмно-бурого или
чёрного цвета, состоящие из неправильных зёрен алмаза с большим количеством
чёрных включений графита и др. примесей.
КАРБОНАРИИ (от итал. carbonaro, букв.- угольщик, от лат. carbo -
уголь), члены одноимённого тайного политич. об-ва, возникшего на Юге Италии в
нач. 19 в., в эпоху наполеоновского господства. Название связано с легендой о
происхождении К. от ср.-век. угольщиков.
После 1815 движение К. распространилось во всех итал. гос-вах. Особенно
широкого размаха оно достигло в Королевстве обеих Сицилии. В движении
участвовали разнородные социальные силы - от либерального дворянства до низшего
духовенства, крестьян и ремесленников. Руководящей силой движения К. была
буржуазия, а также лица свободных профессий и офицеры. Важнейшими целями
движения К. были нац. освобождение (сначала от франц., а затем от австр. гнёта,
проявлявшегося в той или иной степени по всей Италии) и конституция.
Большинство К. принадлежало к сторонникам конституц. монархии, радикальное
меньшинство выдвигало респ. требования. Структура об-ва К. в основных чертах
повторяла структуру масонской орг-ции с её иерархией, сложной обрядовостью и
символикой. Вначале имелись две гл. степени посвящения -"ученик" и
"мастер", впоследствии число степеней возросло до 9. Низшие ячейки
К.-"дочерние венты"- подчинялись "материнским вентам",
к-рыми, в свою очередь, руководили высокие венты, находившиеся в наиболее
крупных городах Италии. Заседание венты сопровождалось множеством символич.
обрядов: при приёме новых членов разыгрывалась яркая эмоциональная сцена
принесения в жертву Христа, считавшегося покровителем карбонариев, и т. п.
К. возглавляли бурж. революции 1820- 1821 в Королевстве обеих Сицилии и в
Пьемонте. После подавления этих революций австр. войсками последовали жестокие
расправы с К. Однако вскоре в Королевстве обеих Сицилии возродилось т. н.
неокарбонарское движение, существовавшее до кон. 40-х гг. К. участвовали в
революц. восстаниях 1831 в Романье, Парме и Модене.
Под влиянием итал. карбонаризма в 1820-21 возникло движение К. во Франции, в
Швейцарии, на Балканах. Гл. целью франц. К. было свержение династии Буроонов;
все их попытки поднять восстание окончились крахом; К. участвовали в Июльской
революции 1830 и в революц. движении 30-х гг.; затем они влились в тайные респ.
об-ва.
Лит.: Ковальская M. И., Движение карбонариев в Италии. 1808-1821, M.,
1971; Канделоро Дж., История современной Италии, пер. с итал., т. 1 - 2, M.,
1958-61; Берти Дж., Демократы и социалисты в период Рисорджименто. пер. с
итал., M., 1965; L е р г е A., La rivoluzione napoletana del 1820-1821, Roma,
1967; Witt J., Les societes secretes de France et d'ltalie..., P., 1830;
Calmette A., Les carbonari en France sous Ia Restauration "La revolution
de 1848", P., 1912 - 14, annee 9, p. 402-17, annee 10, p. 52-73.
M. И. Ковальская.
КАРБОНАТИЗАЦИЯ, процесс изменения горной породы, приводящий к
образованию карбонатов кальция, магния, железа и др. металлов. К. наиболее
часто подвергаются основные интрузивные и особенно эффузивные породы под
действием гидротермальных растворов, богатых двуокисью углерода. Известны
случаи сильной К. гранодиоритовых пород в связи с процессами, вызывающими
образование месторождений золотых и свинцово-цинковых руд. К процессам К.
должны быть отнесены изменения и самих карбонатных пород как в стадии
диагенеза, так и в последующих стадиях преобразования, особенно в случаях
гидротермального метаморфизма карбонатных пород в связи с магматич.
интрузиями. Иногда процесс К. ультраосновных пород сопровождается образованием
талька, фуксита (хромовая слюда) и в этом случае наз. лиственитизацией. В
отдельных р-нах К. служит поисковым признаком нек-рых полезных ископаемых.
КАРБОНАТИТЫ, горные породы маг-матич. или метасоматич. происхождения,
сложенные в основном карбонатами (кальцитом, доломитом, анкеритом) и
пространственно связанные с массивами ультраосновного - щелочного состава.
Термин "К." введён норв. петрографом В. Брёггером (1921),
предложившим также называть кальцитовые К. с ё в и т а м и, доломитовые -
раухаугитам и, биотитдоломитовые жильные - бефорситами, К. красного цвета (в
к-рых карбонат частично замещён окислами железа, гл. обр. гематитом) -
редбергитами.
Массивы ультраосновных - щелочных пород, среди к-рых встречаются К., как
правило, располагаются вдоль крупных разломов на платформах. Они могут быть
"слепыми", не выходящими на поверхность земли, и
"открытыми", достигая при этом земной поверхности в виде вулканов,
извергающих карбонатитовую лаву (вулкан Ол-Доиньо-Ленгаи в Танзании). По
геофизич. данным, массивы прослеживаются на глубину, измеряемую многими
десятками км. К. слагают центральные участки массивов, образуя штоки и
трубчатые тела площадью от 0,1 до 15-20 км2 и больше, а также
неправильные по форме залежи, ветвящиеся зоны, штокверки, кольцевые, конич. и
радиальные дайки. В массивах открытого типа они выполняют жерла вулканов,
нередко цементируя брекчированные вулканич. породы. При развитии К. по
гипербазитам и ийолитам в отдельных массивах возникают форстерит-апатит-магнетитовые
породы с небольшим кол-вом кальцита (фоскориты, камафориты), к-рые иногда
представляют высококачеств. магнетитовые руды (напр., Ковдор на Кольском п-ове
в СССР) или богатые апатитом породы [массив Пхалаборва (Палабора), ЮАР]. При
развитии К. по нефелиновым сиенитам формируется ореол альбититов часто с
тантало-ниобиевым оруденением.
К. представляют собой многостадийные образования, формирующиеся в интервале
темп-р от 600 до 300° С. К. ранних стадий состоят из кальцита, диопсида или
форстерита, биотита или флогопита, апатита и магнетита и обогащены Ti, Zr, Та,
Nb, U.
К. поздних стадий сложены на 80- 95% доломитом или анкеритом и кальцитом,
реже сидеритом, стронцианитом, содержат щелочные амфиболы, серпентин,
ферроферрифлогопит, эгирин, хлорит, эпидот; характерно появление сульфидов -
пирита, пирротина и др., также флюорита, барита, магнетита, рутила, пирохлора,
луэшита, колумбита, ферсмита, бербанкита, бастнезита, паризита,
карбоцернаита, анкилита и др. Характеризуются высокой концентрацией Sr, Ba, F,
Nb, Ce, Th, Pb, Zn, Mo.
К. и сопутствующие им породы представляют важный тип месторождений полезных
ископаемых. С ними связаны крупные месторождения флогопита и вермикулита
(Ковдор, Тулинское в СССР), железа (Ковдор в СССР; Пхалаборва в ЮАР), фосфора
(Пхалаборва в ЮАР; Сукулу в Уганде и др.), богатые месторождения руд ниобия
(Араша, Бразилия; Луэш, Заир; Ока, Канада и др.), также месторождения тантала
(Нкомбва, Замбия), циркония (Пхалаборва, ЮАР), редких земель (Мрима, Кения),
меди (Пхалаборва, ЮАР), флюорита (Тагна, СССР), цементного и известковистого
сырья (Тороро и Сукулу, Уганда). Кроме того, возможно извлечение из нек-рых
месторождений барита и стронцианита. В условиях гипергенеза на К. развивается
кора выветривания, содержание полезных компонентов в которой (апатита,
пирохлора, бастнезита и др.) повышается в 3-5 раз по сравнению с коренными
породами.
Лит.: Гинзбург А. И. [и др.], Редкометальные
карбонатиты, в кн.: Геология месторождений редких элементов, в. 1, M., 1958;
Гинзбург А. И., Эпштейн E. M., Карбонатитовые месторождения, в кн.: Генезис
эндогенных рудных месторождений, M., 1968; Смирнов В. И., Геология полезных
ископаемых, 2 изд., M., 1969; Карбонатиты, под ред. О. Таттла и Дж. Гиттинса, [пер. с англ.], M., 1969; H е i n r i с h E. W., The geology of carbonatites, Chi.,
1966.
А. И. Гинзбург.
КАРБОНАТЫ, соли угольной кислоты H2CO3.
Различают нормальные (средние) К., с анионом COa2- (напр., K2CO3),
кислые К. (гидрокарбонаты или бикарбонаты), с анионом НСО~3 (напр.,
КНСО3) и основные К. [напр., Cu2(OH)2CO3
- минерал малахит]. В воде растворимы только нормальные К. щелочных металлов,
аммония и таллия. В результате значительного гидролиза растворы их
показывают щелочную реакцию. Наиболее трудно растворимы нормальные К. кальция, стронция,
бария и свинца (2-валентного). Кислые К. хорошо растворимы в воде. При
нагревании К., как правило, разлагаются (СаСОз = = CaO + CO2) ещё до
достижения точки плавления; исключение представляют К. щелочных металлов и
таллия. Гидрокарбонаты при нагревании переходят в нормальные К. (2NaHCO3
= Na2CO3 + + H2O + CO2).
Сильными кислотами нормальные и кислые К. разлагаются с выделением CO2
(K2CO3 + H2SO4 = = K2SO4
+ H2O + CO2). В природе нормальные К. широко распространены,
составляя одну из групп минералов (см. Карбонаты природные). Нек-рые
природные, нормальные и основные, К. являются весьма ценными металлич. рудами;
таковы К. цинка, свинца, меди, железа, марганца и др. Нерудное сырьё -
известняк CaCO3, магнезит MgCO3, витерит BaCO3
употребляют в строит, деле, в производстве огнеупоров, в химич. пром-сти и т.
д. Из синтетич. К. в технике широко применяется сода (Na2CO3
и NaHCOs) и в меньшей степени - поташ K2CO3.
Гидрокарбонаты выполняют важную физиологич. роль, являясь буферными веществами
(см. Буферные системы). Об отдельных К. см. Бария карбонат, Калия
карбонат. Кальция карбонат, Магния карбонат, Натрия карбонат и др.
КАРБОНАТЫ ПРИРОДНЫЕ, группа широко распространённых минералов солей
угольной кислоты H2CO3. В соединении с литофильными (Na,
Ca, Mg, Sr, Ba, TR), а также халькофильными (Zn, Cu, Pb, Bi) элементами
образуют более 80 природных соединений (минералов). В состав К. п. входят один
или два главных катиона с добавочными анионами или без них. Основой структуры
К. п. является плоский треугольник [СОз]2-, у к-рого углерод
находится в тройной координации по отношению к атомам кислорода. Группы [CO3]2-
изолированы и соединяются через катионы или дополнительные анионы (OH)-,
F-, Cl-. Структура К.п. слоистая вследствие листового расположения группы [CO3]2-
(тип кальцита) или цепочечная [тип бастнезита Ce(CO3)F],
когда группа [СОз]2- располагается по оси. Плоские группы [CO3]2-
ориентированы либо в виде параллельных слоев и цепочек, либо по иной симметрии.
Большинство К. п. кристаллизуется в ромбич., моноклинной и гексагональной
(тригональной) системах. К. п. характеризуются твёрдостью от 3 до 5 по
минералогич. шкале, повышенной растворимостью в воде (особенно водные карбонаты
щелочных металлов), лёгкой растворимостью в соляной кислоте, высоким двойным
лучепреломлением, диссоциацией при нагревании. Цвет карбонатных минералов
зависит от присутствия ионов-хромофоров. Карбонаты меди - зелёные и синие,
урана - жёлтые, железа и редких земель - коричневые, кобальта и марганца -
розовые, остальные бесцветны или слабо окрашены.
К. п. образуются в разнообразных условиях: в осадочно-морских (в мор.
отложениях карбонаты кальция слагают огромные толщи известняков частью
биогенного происхождения и доломитов), в гидротермальных рудных
месторождениях (кальцит, сидерит, анкерит), в коре выветривания
(магнезит), в метасоматич. образованиях (магнезит, сидерит), в зоне
окисления полиметаллических месторождений (малахит, азурит, смитсонит,
церуссит). Магматогенным путём возникают карбонатиты, с к-рыми
связаны месторождения апатита и редких земель. Многие К. п. (напр.,
смитсонит, малахит, церуссит, стронцианит, сидерит и др.) используются как руда
на Zn, Pb, Bi, Ba, Sr, Cu, Fe, Mn, редкие земли и др. металлы, как сырьё для
цем. и хим. пром-сти (напр., доломит, магнезит) и как строит, материал
(известняк, мрамор).
КАРБОНИЗАЦИЯ, 1) насыщение к.-л. раствора углекислым газом CO2.
Широко применяется в содовом произ-ве, стр-ве, пивовар, деле и др. 2)
Неправильное назв. способа разрушения растит, материалов (соломы, репейника и
т. п.), содержащихся в рунной шерсти, или разрушения растит, волокон в
полушерсти. К. осуществляется обработкой материалов растворами кислот или
кислых солей.
КАРБОНИЛЫ МЕТАЛЛОВ, соединения металлов с окисью углерода общей
формулы Mem(CO)n. Впервые (в 1890) был открыт карбонил никеля Ni(CO)4.
С тех пор получены карбонилы многих металлов и нек-рых неметаллов. В
зависимости от числа атомов металла в молекуле К. м. могут быть
"одноядерными" и "многоядерными"; известны также смешанные
К. м., напр. [Co(CO)4]2Zn.
O строении К. м. см. Комплексные соединения, Валентность.
Карбонилы никеля, железа, осмия, рутения - жидкости; большинство других К.
м.- кристаллич. вещества. К. м. диамагнитны, весьма летучи, чрезвычайно
токсичны. Для меди, серебра, золота известны лишь карбонилгалогениды, Me(CO)X,
устойчивые только в атмосфере окиси углерода. При нагревании выше определённой
темп-ры К. м. разлагаются с выделением окиси углерода и металла в
мелкодисперсном состоянии. Физич. свойства важнейших К. м. приведены в таблице.
Указанные в таблице К. м. хорошо растворимы в органич. растворителях.
Физические свойства некоторых карбонилов металлов
Общий способ получения К. м. заключается во взаимодействии окиси углерода с
металлами или их солями при повышенных темп-pax и давлении. Наибольшее технич.
значение имеют карбонилы никеля Ni(CO)4, кобальта Co(CO)4
и железа Fe(CO)5. Карбонилы применяют для получения чистых металлов,
образующихся при их термич. разложении. Термич. разложение карбонилов
кобальта, никеля и хрома используется для нанесения металлич. покрытий,
особенно на поверхности сложной формы. Карбонилы кобальта и никеля применяются
в качестве катализаторов важных хим. процессов. Их используют при синтезе
карбоновых кислот и их производных из олефи-нов, акриловой кислоты из
ацетилена, при гидроформилировании:
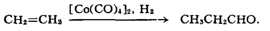
К. м.- хорошие антидетонаторы моторного топлива, однако при их сгорании
образуются трудноудаляемые окислы. Нек-рые карбонилы используются для получения
совершенно чистой окиси углерода.
Лит.: Белозерской H. А., Карбонилы металлов, M., 1958; Химия
координационных соединений, ред. Дж. Бейлар, Д. Буш, пер. с англ., M., 1960;
Химия металлоорганических соединений, под ред. Г. Цейсса, пер. с англ., M.,
1964, с. 538- 604.
H. А. Несмеянов.
КАРБОНИЯ ИОНЫ, карбкатионы, молекулярные частицы, содержащие
трёхковалентный положительно заряженный атом углерода. К. и. обладают высокой
реакц. способностью и поэтому малоустойчивы (ср. Карбанионы). К. и.
образуются:
При гетеролитическом разрыве связи С - X (электронная пара, осуществляющая
эту связь, уходит вместе с группой X):
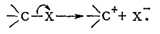
Напр., действие сильных кислот на трифенилкарбинол даёт соль
трифенилметилкатиона:
Этот К. и. устойчив вследствие распределения положит, заряда между неск.
атомами углерода.
При действии апротонных K-T на галогенпроизводные, напр.:
CCl4+AlCl3
<-> CCb++AlCl4-.
При присоединении протона или другого катиона по кратной связи:
(CHO2C=CH2+H+<-> (СН3)3С+
и др. способами.
К. и. легко реагируют с анионами, с молекулами, имеющими неподелённую
электронную пару или кратную связь, и с др. соединениями, атакуя места с
повышенной электронной плотностью. К. и.- промежуточные частицы в большом числе
теоретически и практически важных органич. реакций (напр., алкилирование и
ацилирование по Фриделю - Крафтсу, реакции электрофильного присоединения к
олефинам, изомеризация и катионная полимеризация олефинов, пинаколиновая и
ретропинаколиновая, Демьянова и Вагнера - Меервейна перегруппировки).
Лит.: Бреслоу Р., Механизмы органических реакций, пер. с
англ., M., 1968; Роберте Дж.,Касерио M., Основы органической химии, пер. с
англ., ч. 1 - 2, M., 1968.
Б. Л. Дяткин.
КАРБОНОВЫЕ КИСЛОТЫ, класс органических соединений, содержащих
карбоксильную группу (карбоксил)
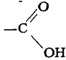
В зависимости от природы радикала, связанного с группой - COOH, К. к. могут
принадлежать к алифатич. (жирному), алициклич., ароматич. или гетероциклич.
ряду. По числу карбоксильных групп в молекуле различают одно-, двух- и
многоосновные (соответственно моно-, ди- и поликарбоновые) кислоты. Кроме того,
К. к. могут быть насыщенными (предельными) и ненасыщенными (непредельными),
содержащими в молекулах двойные или тройные связи. Большинство К. к. имеет
тривиальные названия, многие из к-рых связаны с их нахождением в природе, напр,
муравьиная, яблочная, валериановая, лимонная к-ты. По Женевской номенклатуре
наименования К. к. производят от названий углеводородов с тем же числом атомов
углерода, прибавляя окончание "овая" и слово "кислота", напр,
метановая к-та (муравьиная), этановая к-та (уксусная) и т. д. Нередко К. к.
рассматривают как производные углеводородов; напр., кислоту строения HC = С -
COOH наз. ацетиленкарбоновой к-той.
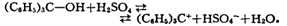
Кислотные свойства обусловлены способностью К. к. к диссоциации в водном
растворе:
RCOOH <->± RCOO-+H+.
Как правило, К. к. слабее минеральных. Константы диссоциации одноосновных
насыщенных кислот жирного ряда при 25 0C изменяются от 1,7-10-4
(муравьиная к-та) до 1,3-10~5 (высшие гомологи). Сила К. к.
существенно зависит также от электрофильности радикала, связанного с
карбоксилом. Введение электроотрицат. заместителей (напр., NO2, CN, Cl)
в положение, соседнее с карбоксильной группой, резко повышает кислотность,
напр, аиануксусная к-та CNCH2COOH примерно в 200 раз сильнее
уксусной к-ты CH3COOH. По мере удаления от карбоксила влияние
заместителей ослабевает. Дикарбоновые к-ты сильнее монокарбоновых, причём
влияние одного карбоксила на другой тем больше, чем они ближе расположены друг
к другу. Так, в ряду кислот щавелевая кислота HOOC - COOH сильнее малоновой
к-ты HOOCCH2COOH, к-рая, в свою очередь, сильнее янтарной НООС(СН2)2СООН,
и т. д. Кислотность непредельных K-T выше, чем предельных; влияние двойной
связи тем сильнее, чем она ближе расположена к карбоксилу. Так, акриловая к-та
CH2 = CH -COOH в 4 раза сильнее пропионовой СНз - CH2 -
COOH. Ароматич. кислоты сильнее предельных алифатических (напр., константа
диссоциации бензойной кислоты 6,5-10-5).
К. к.- жидкие (напр., низшие жирные к-ты) или твёрдые (напр., высшие жирные
и ароматич. к-ты) вещества (см. табл.). Низшие члены насыщенных К. к. жирного
ряда хорошо растворимы в воде, средние члены (C4 - C10),
а также ароматич. к-ты - ограниченно, высшие жирные кислоты в воде не
растворимы; как и ароматич. к-ты, они хорошо растворяются в спирте, эфире,
бензоле.
Наиболее важные хим. свойства К. к.- способность превращаться в производные.
При взаимодействии с основаниями К. к. дают соли: RCOOH + NaOH ->
->RCOONa + H2O. При действии на К. к. спиртов в присутствии
минеральных K-T легко образуются эфиры сложные: RCOOH + R'OH ->RCOOR'
+ H2O; при действии галогенангидридов минеральных K-T (напр.,
PCl3,POCl3, SOCl2)-галогенангидриды К. к. RCOX
(X - атом галогена). При нагревании кислот с водоотнимающими средствами
получаются ангидриды К. к. (RCO)2O. Галогенангидриды и ангидриды К.
к. применяют как ацилирующие агенты. Отщепление воды от аммониевых солей К. к.
(1) и реакция галогенангидридов с аммиаком (2) приводят к амидам кислот:
1) RCOONH4 ->
RCONH2-I-H2O 2) RCOC1+2NH3 -> RCONH2-WH4Cl.
Методы получения К. к. весьма многочисленны. Окислением первичных спиртов и
альдегидов получают К. к. с тем же числом атомов углерода. Окисление ке-тонов
сопровождается разрывом связи С - С; из циклич. кетонов образуются дикарбоновые
к-ты, напр, адипиновая кислота из циклогексанона:
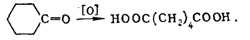
Насыщенные углеводороды м. б. подвергнуты деструктивному окислению с
образованием смеси продуктов, в том числе и карбоновых K-T. Этим методом из 1 m
парафина обычно получают ок. 350 кг К. к. Окисление боковой цепи
жирно-ароматич. углеводородов либо многоядерных ароматич. углеводородов
приводит к ароматич. К. к.; напр., фталевая к-та получается окислением
о-ксилола или нафталина:
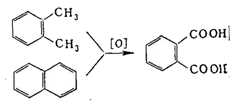
Ненасыщенные углеводороды окисляются по месту двойной связи:
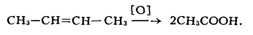
Важный метод синтеза К. к.- гидролиз их нитрилов, легко получаемых взаимо-
Некоторые представители карбоновых кислот и их свойства
|
|
|
|
|
|
Алифатические (жирные) кислоты
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH1(CH2)7CH = =СН(СН2)7СООН
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
* В скобках указана темп-pa (в 0C). ** 1 мм рт. с.т. =
133. 322 н/м2.
действием галогенопроизводных углеводородов с цианистым натрием:
RCl + NaCN -> RCN ->
RCOOH. В наст, время пром. значение приобрёл метод синтеза К. к. карбонилированием,
т. е. введением группы СО в органич. соединения:
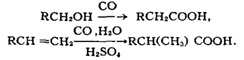
Нек-рые К. к. получают из природных продуктов. Так, щелочным гидролизом
(омылением) жиров получают соли высших жирных кислот (мыла) и глицерин.
Лимонную к-ту получают из ботвы хлопчатника и из стеблей махорки (после
выделения из них никотина). Многие К. к. получают сбраживанием углеводов в
присутствии бактерий определённого вида (маслянокислое, молочнокислое,
лимоннокислое и др. виды брожения).
К. к. широко распространены в природе в свободном состоянии и в виде
производных (гл. обр. сложных эфиров). Так, в летучем масле герани содержится
пеларгоновая к-та, в лимонах - лимонная. В состав животных и растит, жиров и
масел входят глицериды высших нормальных К. к. жирного ряда, из которых
преобладают пальмитиновая кислота, стеариновая кислота и олеиновая
кислота.
К. к., их производные, а также многочисл. соединения, содержащие наряду с
карбоксильной иные функциональные группы (напр., аминокислоты, оксикислоты и
др.), имеют большое биологич. значение и находят разнообразное практич.
применение. Муравьиную и уксусную к-ты, напр., применяют при крашении и
печатании тканей; уксусную к-ту и уксусный ангидрид - в произ-ве ацетилцеллюлозы.
Аминокислоты входят в состав белков. В медицине используют салициловую
к-ту, п-аминосалициловую к-ту (ПАСК) и др.
Высшие жирные К. к. широко применяют как сырьё для произ-ва мыла, лаков и
красок, поверхностно-активных веществ, как эмульгаторы в произ-ве
кау-чуков, как пластификаторы в произ-ве резин и др. Адипиновая к-та - один из
исходных продуктов в произ-ве полиамидного волокна (найлона),
терефталевая - в производстве полиэфирного волокна (лавсана, терилена), полимерный
нитрил акриловой к-ты (орлон) применяют как синтетич. волокно, близкое по
свойствам к натуральной шерсти. Полимеры и сополимеры эфиров метакриловой к-ты
используют как органич. стекло.
Лит.: Неницеску К. Д., Органическая химия, пер. с рум., т. 1 - 2, M.,
1962- 1963; Несмеянов A. H., Несмеянов H. А., Начала органической химии, кн. 1
- 2, M., 1969 - 70.
КАРБОРАНЫ, химич. соединения, состоящие из атомов бора, углерода и
водорода, общей формулы BnCmHn+m. B К. атомы В
и С расположены по вердшинам более или менее правильного многогранника, причём
каждый атом В или С связан с одним атомом H. В К. один из атомов В или С может
быть замещён на атом другого элемента, напр, фосфора, мышьяка, олова, алюминия
и т. д. Агрегатное состояние К. по мере увеличения п меняется от
газообразного до твёрдого. К. и их производные отличаются высокой термич. и
хим. стабильностью. По свойствам они во многом аналогичны ароматич.
углеводородам и способны к разнообразным превращениям, к-рые связаны с
замещением атомов H, стоящих у атома С или В. К. получают в основном
взаимодействием производных ацетилена с соответствующими бороводородами.
Карборан B10C2H12 применяют для получения
различного типа полимеров, используемых в твёрдых ракетных топливах и в
качестве термостойких покрытий.
Лит.: Михайлов Б. M., Химия боро-водородов, M., 1967; Жигач А.
Ф., Стасиневич Д. С., Химия гидридов, Л., 1969.
H. И. Бекасова.
КАРБОРУНД, SiC, соединение кремния с углеродом; то же, что кремния
карбид.
КАРБОТЕРМИЯ (от карбо... и греч. therme - теплота, жар),
металлургич. процессы, основанные на восстановлении металлов из их соединений
углеродом и углеродсодержащими материалами при повышенных темп-pax. Наиболее
распространённый углеродсодержащий материал - металлургический кокс. Различают
прямое восстановление (твёрдым углеродом) и косвенное (окисью углерода).
Карботермич. восстановление лежит в основе металлургии железа (см. Доменное
производство). В цветной металлургии с помощью К. получают свинец, олово,
значит, часть цинка и нек-рые др. металлы.
Лит.: Есин О. А. и Г е л ь д П. В., Физическая химия металлургических
процессов, ч. 1, Свердловск, 1962.
КАРБОТИОН, карбатион, N-метилдитиокарбамат натрия, хим. средство
борьбы с почвенными возбудителями болезней растений и сорняками (см.
Стерилизаторы почвы).
КАРБОФОС, О,О-диметил-8-1,2-дикарбоэтоксиэтилдитиофосфат, химич.
средство борьбы с вредными насекомыми. См. Инсектициды.
КАРБОЦЕПНЫЕ ПОЛИМЕРЫ, полимеры, основная цепь макромолекул
к-рых построена только из атомов углерода.
КАРБОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ (от карбо... и греч. kyklos -
круг, кольцо), изоциклические соединения, органич. соединения, содержащие в
молекулах кольца (циклы) из атомов углерода. К. с. отличаются от гетероциклических
соединений, циклы к-рых содержат, кроме атомов углерода, атомы др.
элементов, чаще всего О, N или S, а также от ациклических соединений, не
содержащих циклов. К. с.- один из осн. классов органич. соединений, к-рый
подразделяют на алициклические соединения и ароматические соединения (бензоидного
и небензоидного характера). К. с. чрезвычайно распространены; многие из них
имеют большое практич. значение. Так, к ним относится значит, часть
углеводородов нефти, терпенов, ряд антибиотиков, многие красители, лекарств,
вещества, инсектициды и др.; их применяют для получения синтетич. смол,
пластич. масс и т. д.
КАРБРОМАЛ, адалин, лекарственный препарат из группы снотворных
средств. Применяют в порошках и таблетках как успокаивающее при
неврастении, истерии, различных заболеваниях нервной системы; как снотворное -
при затруднённом засыпании, повышенно чутком сне. Противопоказание - повышенная
чувствительность к брому.
КАРБУНКУЛ (лат carbunculus, букв.- уголёк; старинное рус. назв.-
огневик, углевик), острое гнойно-некротич. воспаление кожи и подкожной
клетчатки вокруг группы волосяных мешочков и сальных желез, имеющее тенденцию к
быстрому распространению. К. располагаются обычно на задней части шеи, на лице,
пояснице, спине; возникают чаще всего при загрязнении кожи в местах трения её
одеждой, вследствие попадания гноеродных микробов (стафи-ло- и стрептококков).
Возникновению и развитию К. способствуют истощение, сах. диабет, нарушения
деятельности желудочно-кишечного тракта, печени и почек. Кожа в месте поражения
воспалённая, багрово-синяя; процесс протекает с нагноением. При отторжении
омертвевших участков в коже образуется множество воронкообразных отверстий,
затем - рана с грязно-серым дном и подрытыми краями. К. сопровождается общей
интоксикацией, высокой темп-рой, в тяжёлых случаях - рвотой, потерей сознания.
Л е ч е н и е: покой, обкалывание К. новокаином с антибиотиками,
рентгенотерапия, УВЧ, переливание крови, высококалорийная диета; в стадии
некроза - хирургия, операция. Профилактика: гигиенич. содержание кожи и белья.
А. Б. Галицкий.
KAPБУНСКИЙ КЛАД, комплекс предметов раннего этапа триполъской
культуры, найден в 1961 на месте трипольско-гопоселения ус. Карбуна, ныне
Новоанненского р-на Молд. CCP. Это единственная находка такого клада в Вост. Европе. В глиняном сосуде, прикрытом сверху др.
сосудом, находились медные топоры, пластинчатые и спиральные браслеты, бусы,
антропоморфные фигурки; топоры и бусы из цветного мрамора и камня, амулет из
зуба человека, костяная жен. фигурка, бусы и декоративные пластины из мор.
раковин. Ритуальное назначение нек-рых предметов позволяет предположить, что
владельцем клада был племенной вождь и жрец.
Лит.: Сергеев Г. П., Раннетрипольский клад у села Карбуна,
"Советская археология", 1963, № 1.
Э. А. Рикман.
КАРБЫШ, название двух различных видов грызунов: суслика-песчаника
(Ci-tellus fulvus) и хомяка обыкновенного (Cricetus cricetus). См. Суслики,
Хомяки.
КАРБЫШЕВ Дмитрий Михайлович [14(26).10.1880, Омск,-18.2.1945,
Австрия, лагерь смерти Маутхаузен], советский военачальник, ген.-лейтенант инж.
войск (1940), проф., доктор воен. наук (1941), Герой Сов. Союза (16.8.1946).
Чл. КПСС с 1940. Род. в семье воен. чиновника. Окончил Николаевское инж. уч-ще
(1900) и Николаевскую инж. акад. (1911). Участвовал в рус.-япон. войне 1904-05.
С 1911 руководил стр-вом фортов Брестской крепости. Во время 1-й мировой войны
1914-18- в управлении начальника инж. войск 11-й и 8-й армий, последний чин -
подполковник. С дек. 1917 отрядный инженер Красной Гвардни в Могилёве-Подольском. В Гражданскую войну 1918-20 организовывал инж.
обеспечение операций по разгрому войск Колчака и Врангеля. В 1921-23 на
ответств. должностях в штабе вооруж. сил Украины и Крыма и Укр. воен. округа.
В 1923-26 пред. Инж. к-та Гл. воен.-инж. управления РККА. С 1926 на
преподават. работе в Воен. академии им. Фрунзе, с 1936 в Воен. академии
Генштаба. Автор мн. науч. трудов: "Инженерная подготовка границ СССР"
(кн. 1, 1924), "Разрушения и заграждения" (1931, совм. с И. Киселёвым
и И. Масловым), "Инженерное обеспечение боевых действий стрелковых
соединений" (ч. 1-2, 1939- 1940) и др. К. разработал основы теории инж.
обеспечения операций и боевого применения инж. войск. В начале Великой
Отечественной войны 1941-45, находясь на фронте (Зап. Белоруссия), 8 авг. 1941
был тяжело контужен и попал в плен. Вёл антифашистскую агитацию среди пленных в
лагерях смерти (Замосць, Майданек и др.), был зверски замучен фашистами.
Награждён орденом Ленина (посмертно), до войны - орденами Красного Знамени,
Красной Звезды и медалью 20 лет РККА. К. установлены памятники в Маутхаузене,
Омске, Таллине.
Соч.: Избр. научные труды, M., 1962.
Лит.: Солдат, герой, ученый, M.,
1961.
А. И. Иволгин, В. А. Пурин.
КАРБЮРАТОР (от франц. carburateur), прибор для дозировки топлива и
приготовления горючей смеси из жидкого топлива и воздуха для питания двигателя
внутреннего сгорания с внешним смесеобразованием. Процесс приготовления
горючей смеси наз. карбюрацией. Для того чтобы топливо в цилиндрах сгорало
полностью с большой скоростью, выделяя при этом возможно большее кол-во тепла,
оно должно быть подготовлено к сгоранию. Подготовка смеси заключается в том,
что жидкое топливо раздробляется на мелкие капельки (распыливается), интенсивно
перемешивается с воздухом и испаряется. Распыливание топлива в К. происходит в
результате попадания тонкой струи топлива, вытекающего из распылителя, в
быстродвижущийся поток воздуха, к-рый разбивает струю топлива на мелкие капли,
смешивается с ним и увлекает топливо по впускному трубопроводу в цилиндры
двигателя.
По направлению воздушного потока К. делятся на 3 группы: с падающим
(нисходящим) потоком, с восходящим и с горизонтальным. К. с нисходящим потоком
получили преим. распространение на автомобильных двигателях. К. с
горизонтальным потоком применяются гл. обр. на мотоциклах, лодочных двигателях,
а также на форсированных автомобильных двигателях.
К. (рис.) присоединяется к впускному трубопроводу двигателя. Во время такта
впуска поршень движется от головки цилиндра, в результате чего в цилиндре
создаётся разрежение, поэтому наружный воздух устремляется в цилиндр и, проходя
с большой скоростью через смесит, камеру К., увлекает за собой топливо.
Количество подаваемой в цилиндр горючей смеси регулируют дроссельной заслонкой.
Простейший К. не обеспечивает требуемого изменения состава горючей смеси при
переходе от одного режима работы двигателя к другому. Для обеспечения
необходимого качества состава смеси на всех режимах работы К. имеют дозирующие
устройства с автоматич. регулированием. График изменения состава горючей смеси,
подаваемой в двигатель в зависимости от расхода воздуха или нагрузки двигателя,
наз. характеристикой К.
Схема простейшего карбюратора: 1 - смесительная камера;
2 - диффузор; 3 - воздушный
патрубок; 4 - воздушная заслонка; 5 - топливопровод; 6 - отверстие,
соединяющее поплавковую камеру с атмосферой; 7 - запорная игла; 8 - поплавок;
9 - поплавковая камера; 10 - жиклер; 11 - распылитель; 12 - дроссельная
заслонка.
Регулировка К. и его технич. состояние существенно влияют на работу
двигателя. Нарушение регулировки К. приводит к ухудшению экономичности,
ди-намич. качеств автомобиля, а также к увеличению токсичности отработавших
газов.
Лит.: Грибанов В. И., Орлов В. А., Карбюраторы двигателей внутреннего
сгорания, 2 изд., Л., 1967; Б л е й з H. Г., Автомобильные карбюраторы,
бензонасосы, фильтры, M., 1967.
Б. А. Куров.
КАРБЮРАТОРНЫЙ СКРАП-ПРОЦЕСС, процесс выплавки стали в мартеновских
или электросталеплавильных печах, при к-ром углерод вводится в шихту не с
чугуном, а с высокоуглеродистыми материалами - карбюраторами: коксом,
антрацитом, каменным углем, древесным углем и др. При выплавке стали этим
способом металлич. часть шихты состоит только из стального лома, в отличие от
др. разновидностей мартеновского процесса, когда в шихту входит 30-80% чугуна.
При т. н. полукарбюраторном процессе металлич. шихта содержит небольшое кол-во
чугуна (3-5% ), остальное - стальной лом. Тот и другой процессы применяются
ограниченно - при отсутствии или недостатке чугуна в данном экономич. районе. К
недостаткам К. с.-п. относятся: меньшая, по сравнению с др. видами
мартеновского процесса, производительность печи; сокращённый срок её службы
(из-за большего расхода тепла и большей длительности расплавления шихты);
увеличенный расход топлива и раскислителей; как правило, повышенное содержание
в стали серы (попадающей в неё из карбюратора). См. также Мартеновское
производство.
KAPВАШ (Karvas) Петер (р. 25.4.1920, Банска-Бистрица), словацкий
писатель, драматург. Участник Словацкого нац. восстания 1944. Учился в Карловом
(Прага) и Братиславском ун-тах. Печататься начал в 1938. Теме антифаш. борьбы
словацкого народа поев, драматургич. трилогия "Метеор" (1945, рус.
пер. 1958), "Бастион" (1948), "Возвращение к жизни" (1949)
и др. произв.- драмы "Полуночная месса" (1959, рус. пер. 1960),
"Антигона и другие" (1961), романы, рассказы. Морально-этические
проблемы социалистического общества - в центре второй "трилогии" К.
("Люди с нашей улицы", 1951, рус. пер. 1960, "Сердце, полное
радости", 1954, "Пациент 113", 1955, рус. пер. 1957) и пьесы
"Язва" (1963). К. выступает также в жанрах философско-драматич.
памфлета, сатирич. рассказа, юморески.
Соч.: Toto pokolenie, 2 vyd., Brat., 1955;
Pokolenie v utoku, 2 vyd., Brat., 1956; Kniha ul'avy. Brat., 1970; в
рус. пер.- Чёрт не дремлет. Очерки. Фельетоны, M., 1957; Сотрудник загрустил,
M., 1960.
KAPBEP (Carver) Томас Никсон (25.3. 1865, Керквилл, штат Айова,-
1961, Санта-Моника, штат Калифорния), американский экономист. Представитель
вульгарной буржуазной политич. экономии. В 1891 окончил Калифорнийский ун-т.
Доктор философии (1894), проф. экономики Гарвардского ун-та (с 1902). К.-
последователь теории предельной производительности Дж. Б. Кларка, к-рой
он пытался придать более конкретный характер путём использования матема-тич.
аппарата. Утверждал, что в США наступила эпоха постоянного процветания,
стираются различия между рабочими и предпринимателями, призывал рабочих к
отказу от борьбы с капиталом и сотрудничеству с предпринимателями. Антинаучные
концепции К. стали исходными для "народного" капитализма теории.
Соч.: The distribution of
wealth, N. Y., 1904; Principles of political economy, Boston, 1919; The present
economic revolution in the United States, Boston, 1925; Recollections of an
unplanned life, Los Ang., 1949.
В. Г. Сарычев.
КАРВИНА (Karvina), город в Чехословакии, в Чешской Социалистич.
Республике, в Сев.-Моравской обл. 77,1 тыс. жит. (1970). Один из осн. центров
добычи угля в Остравско-Карвинском кам.-уг. басс.; произ-во кокса,
металлообработка. ТЭЦ.
КАРГАЛА, посёлок гор. типа в Оренбургском р-не Оренбургской обл.
РСФСР. Ж.-д. станция в 20 км от Оренбурга. В районе К. осваивается
крупное газоконденсатное месторождение; строятся (1973) газоперерабатывающие
з-ды.
КАРГАЛИНСКИЙ КЛАД, женское погребение (возможно, шаманки) с богатым
инвентарём 2 в. дон. э.- 2 в. н. э., открытое в 1939 при земляных работах в
ущелье р. Каргала близ г. Алма-Ата. В погребении найдено около 300 золотых предметов:
перстни, серьга, рельефные бляшки и др. Наиболее интересна диадема в форме
прямоугольной ажурной пластины с изображением охотничьей сцены (на фоне растит,
орнамента - люди и животные, в т. ч. фантастич. дракон и крылатые кони).
Характер головных уборов на человеческих фигурах, нек-рые изображения животных,
а также особенности ювелирной техники свидетельствуют о местном происхождении
вещей К. к.
Лит.: Бернштам A.H., Золотая диадема из шаманского погребения на р.
Кара-галинке, в сб.: Краткие сообщения о докладах и полевых исследованиях
Института истории материальной культуры, [в.] 5, М.- Л., 1940; его же, Прошлое
района Алма-Ата, А.-А., 1948.
КАРГАПОЛОВ Михаил Иванович (р. 9.11.1928, дер. Русакова Курганской
обл.), советский математик, чл.-корр. АН СССР (1966). Чл. КПСС с 1965. Окончил
Уральский (Свердловск) ун-т (1951), с 1964 проф. Новосибирского ун-та. Осн.
труды, относящиеся к алгебре, посвящены гл. обр. исследованию свойств
бесконечных дискретных групп, в том числе обобщённо разрешимых и
упорядочиваемых групп, а также исследованию алгоритмич. проблем. Награждён
орденом Трудового Красного Знамени и медалями.
Лит.: Математика в СССР. 1958-1967, т. 2, M., 1969 (имеется библ.).
КАРГАПОЛЬЕ, посёлок гор. типа, центр Каргапольского р-на Курганской
обл. РСФСР. Расположен на р. Миасс (басе. Оби), в 17 км к С.-В. от ж.-д.
станции К. (на линии Курган - Свердловск) и в 111 км к С.-З. от Кургана.
Ремонтно-механич. и кирпичный з-ды, маслозавод.
КАРГАСОК, посёлок гор. типа, центр Каргасокского р-на Томской обл.
РСФСР. Пристань на лев. берегу Оби, в 535 км к С.-З. от Томска.
Леспромхоз, рыбозавод, маслодельный з-д, мясо-молочный и откормочный совхозы. В
районе - лесная пром-сть, месторождения нефти и газа.
КАРГАТ, река в Новосибирской обл. РСФСР, прав, приток р. Чулым (басс.
оз. Чаны). Дл. 387 км (от истока р. Каргатёнок), пл. басе. 7,2 тыс. км2.
Протекает по Барабинской низм. Питание в основном снеговое. Cp. годовой
расход воды у с. Ниж. Каргат (36 км от устья) 8,54 м3/cек.
Замерзает в ноябре, вскрывается во 2-й пол. апреля. На реке - г. Каргат.
КАРГАТ, город (до 1965 - посёлок), центр Каргатского р-на
Новосибирской обл. РСФСР. Расположен на р. Каргат. Ж.-д. станция на линии
Барабинск - Новосибирск. Маслосыродельный и мясной комбинаты.
КАРГЕР Михаил Константинович [р. 17(30).5.1903, Казань], советский
археолог и искусствовед, специалист по славяно-рус, археологии и истории
др.-рус. культуры и иск-ва, доктор ист. наук (1959). Окончил Петроградский ун-т
(1923). Проф. Ленингр. ун-та (с 1949), зав. Ленингр. отделением Ин-та
археологии АН СССР (с 1964). Руководитель археологич. и реставрац. работ в
Новгороде, Киеве, Переяславе-Хмельницком, Галиче, Владимире-Волынском,
Полоцке, Турове, Изяславле и др. городах. Гос. пр. СССР (1952). Награждён
орденом Ленина.
Соч.: Древний Киев, т. 1-2, М.- Л., 1958-61; Новгород Великий, М.- Л., 1961;
Зодчество древнего Смоленска (XII - XIII вв.), Л., 1964.
Лит.: В а г н е р Г. К., Кирпичников A. H., К 60-летию M. К.
Каргера,"Советская археология", 1963, № 4.
КАРГИH Валентин Алексеевич [10 (23).1.1907, Екатеринослав, ныне
Днепропетровск,- 21.10.1969, Москва], советский химик, акад. АН СССР (1953;
чл.-корр. 1946). Герой Социалистич. Труда (1966). Окончил Моск. ун-т (1930);
работал в Физико-химическом ин-те им. Л. Я. Карпова (с 1930) и МГУ (1956-
1969). Один из создателей сов. науч. школы по физико-химии полимеров. Осн.
труды посвящены механизму образования коллоидных систем и, особенно,
физико-химии высокомолекулярных соединений. К. показал, что растворы полимеров
- термодинамически обратимые системы. Исследовал закономерности механич. и
термомеханич. свойств полимеров, связь между физико-хим. свойствами полимерных
материалов и их строением на молекулярном и надмолекулярном уровнях; эти работы
привели к нахождению эффективных способов структурно-хим. и физ. модификации
пластмасс, каучуков и хим. волокон. К. исследовал роль структурных
характеристик реакц. среды в образовании макромолекул. Основал (1956) в МГУ
первую в СССР университетскую кафедру высокомолекулярных соединений. Гл.
редактор журн. -"Высокомолекулярные соединения" (1959-69).
Работы К. нашли широкое применение в пром-сти. Ленинская пр. (1962), Гос. пр.
СССР (1943, 1947, 1950, 1969). Награждён 3 орденами Ленина, 2 др. орденами, а
также медалями. Портрет стр. 409.
Соч.: Краткие очерки по физико-химии полимеров, 2 изд., M., 1967 (совм. с Г.
Л. Слонимским).
Лит.: Валентин Алексеевич Каргин, M., 1960 (АН СССР. Материалы к
биобиблиографии ученых СССР. Сер. химических наук, в. 29).
КАРГОПОЛЬ, город, центр Каргопольского р-на Архангельской обл. РСФСР.
Расположен на лев. берегу р. Онеги, в 5 км от её истока из оз. Лача, в
89 км к 3. от ж.-д. ст. Няндома (на линии Вологда - Архангельск).
Известен с 14 в. В 15-16 вв. значит, торг, поселение (торговля солью). В 1608 в
К. был сослан И. И. Болотников; здесь его ослепили и утопили в Онеге. В
1612 К. выдержал осаду поляков. С 1801 уездный город Олонецкой губ. В К.-з-ды:
маслодельный, пивовар., льнообрабат., асфаль-тобетонный. Архитектурные
памятники: Христорождественский собор (1562), церкви Благовещения (1682-92),
Владимирская (1653), Рождества богородицы (1653), Иоанна Предтечи (1751) - кам.
кубич. храмы с 4-скатными крышами; на фасадах - декор в "узорочном
стиле". Пед. училище. Краеведч. музей.
Каргополь. Церковь Рождества богородицы. 1653.
Лит.: Гемп К. П., Каргополь, Архангельск, 1968; Бартенев И., Фёдоров
Б., Архитектурные памятники русского Севера, Л.- M., 1968, с. 103-115.
KAPГОПОЛЬСКАЯ КУЛЬТУРА, археол. культура племён охотников и
рыболовов, живших в р-не озёр Лача, Воже, Кенозеро и отчасти Белого (совр.
Вологодская и Архангельская обл. РСФСР). Названа по месту осн. находок на терр.
Каргопольского р-на Архангельской обл. РСФСР. Древнейшие памятники относятся к
концу мезолита и характеризуются грубыми кремнёвыми орудиями, костяными
наконечниками стрел и пр. В 4-м тыс. до н. э. появляется керамика с орнаментом
из крупных ямок, сменяющаяся керамикой с ямочно-гребенчатым орнаментом;
кремнёвые орудия приобретают неолитич. облик, появляются кам. фигурки животных
и изображения человека из глины. В кон. 2-го тыс. до н. э. преобладает гладкая
и сетчатая керамика, кремень почти выходит из употребления.
Лит.: Ф о с с M. E., Древнейшая история севера Европейской части
СССР, в сб.: Материалы и исследования по археологии СССР, № 29, M., 1952.
КАРДАМОН (Elettaria cardamomum), многолетнее травянистое растение сем.
имбирных с ползучим корневищем. Листья ланцетовидные, двурядно расположенные на
вегетативных побегах выс. 2-4 м. Цветоносные побеги вые. до 60 см заканчиваются
метёлками с бледно-зелёными цветками. Плод - трёхгнёздная коробочка с
красновато-бурыми семенами неправильной формы. Семена используются в кулинарии
как пряность, содержат 3,5-7% масла, применяемого в пищ. и табачной пром-сти, а
также в медицине. К. растёт во влажных горных лесах Юж. Индии; культивируют его
гл. обр. в Индии, на Шри-Ланка (Цейлоне), на п-ове Индокитай, в Юж. Китае.
Кардамон; часть корневища с цветоносным побегом и лист; а, б, в - плоды.
КАРДАМОНОВЫ ГОPЫ, горы на крайнем юге Индии, в южной части Зап. Гат.
Выс. до 2019 м (T. Коттаймалай). Для рельефа характерны резкие очертания
гребня, крутые склоны, глубокие ущелья. Сложены преим. гнейсами, кристаллич.
сланцами, чарнокитами. Покрыты влажными тропич. лесами. Чайные и каучуковые
плантации. Произ-во пряностей.
КАРДАННАЯ ПЕРЕДАЧА автомобиля (от имени Дж.
Кардана), устройство
для передачи вращения от ведущего вала к ведомому, расположенных под углом один
к другому. Часто в процессе работы угол и расстояние между валами непрерывно
изменяются. В автомобилях К. п. (рис. 1) применяются для соединения двигателя и
коробки передач (угол до 5°), коробки передач с раздаточной коробкой (угол до
5°), коробки передач (раздаточной коробки) с главной передачей (угол до 15°), а
также в др. случаях (в рулевом приводе, для привода лебёдок и т. п.). К. п.
включает карданный вал с двумя (реже одним) карданами. Если карданным валом
соединяются механизмы, угол и расстояние между к-рыми изменяются (напр.,
коробка передач и гл. передача автомобиля), предусматривается осевая
компенсация в виде скользящего шлицевого соединения, допускающего изменение
длины вала в заданных пределах. В зависимости от величины угла между валами в К.
п. могут быть использованы полукарданы (жёсткие или упругие), полные карданы
неравных угловых скоростей или карданы равных угловых скоростей. Наиболее
распространены полные карданы (рис. 2), осн. деталями к-рых являются две вилки,
игольчатые подшипники, крестовина, опоры для цапф крестовины и уплотняющие
устройства. Кпд одного кардана - 0,985-0,99.
Лит.: M а л а х о в с к и й Я. Э., Лапин А. А., Веденеев H. К.,
Карданные передачи, M., 1962.
M. И. Лурье.
Рис. 1. Схема карданной передачи автомобиля:
1 - коробка передач; 2 - кардан;
3 - скользящее шлицевое соединение; 4 - карданный вал; 5 -
главная передача.
Рис. 2. Полный кардан: / - вилка; 2 - опора для цапф крестовины; 3
-крышка; 4 - крестовина.
КАРДАННЫЙ МЕХАНИЗМ, кардан, карданный или универсальный шарнир,
шарнирная муфта, механизм, обеспечивающий вращение двух валов под переменным
углом, благодаря подвижному соединению звеньев (жёсткий К. м.) или упругим
свойствам спец. элементов (упругий К. м.). К. м. назван по имени Дж. Кардана,
предложившего подвес для сохранения неизменным положения тела при любых
поворотах его опоры. Простым жёстким К. м. является т. н. шарнир Гука (рис.1).
Оси вращения I, II,
III, IV пересекаются под углом а в неподвижной точке
О центра сферы с радиусом OB = OB' = OC= ОС; поэтому при любом значении
угла а в пределах 0°<а<90°шарниры В,В' и C1C` попарно
описывают окружность того же радиуса в плоскостях, перпендикулярных осям I и
II. При этих условиях передача вращения возможна с меняющимся углом а.
Это свойство К. м. обусловило его широкое применение в различных машинах:
летат. аппаратах, приборах, станках (шарнирная муфта), автомобилях (карданная
передача), с.-х. машинах и др., когда по условиям работы необходимо изменение
взаимного расположения валов, передающих вращение.
Рис. 1. Схема шарнира Гука: /, 2 - вилки; 3 - крестовина; В,
В' и С, С' - шарниры, /, II, III, IV - оси вращения.
Рис. 2. Схема двойного шарнира Гука: / - ведущий вал; 2 - промежуточный вал;
3 - ведомый вал; А, В - универсальные шарниры.
Рис. 3. Карданный механизм, действие которого основано на принципе деления
угла между валами биссекторной плоскостью: /, 5 - валы, расположенные в одной
плоскости и пересекающиеся под углом; 2 - направляющий палец,
устанавливающий сепаратор при изменении угла между осями валов; 3-сепаратор;
4- шарики, лежащие в биссекторной плоскости.
Рис. 4. Упругий карданный механизм: / - центрирующий шаровой палец; 2, 4
- валы; 3 - гибкие элементы.
Недостатком простого К. м. является неравномерность скорости вращения
ведомого вала при постоянной скорости ведущего. Изменение скорости ведомого
вала тем больше, чем больше угол 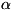 . При
. При 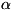 90° передача вращения с помощью простого К. м.
становится невозможной. В этих случаях, а также при необходимости обеспечить
равномерное вращение ведомого вала целесообразно применение двойного К. м.
(рис. 2), в к-ром углы
90° передача вращения с помощью простого К. м.
становится невозможной. В этих случаях, а также при необходимости обеспечить
равномерное вращение ведомого вала целесообразно применение двойного К. м.
(рис. 2), в к-ром углы 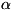 1 и
1 и 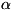 2 равны, а вилки на
валу 2 расположены в одной плоскости. Если вследствие недостатка места
нельзя разместить двойной К. м., используют кардан, устройство к-рого основано
на делении угла между валами биссекторной плоскостью (рис. 3). Угол наклона
валов двойных жёстких К. м. может достигать 38°. При углах наклона валов 3-50
применяют упругий К. м. (рис. 4), гибкие элементы к-рого выполняют из
прочного эластичного материала.
2 равны, а вилки на
валу 2 расположены в одной плоскости. Если вследствие недостатка места
нельзя разместить двойной К. м., используют кардан, устройство к-рого основано
на делении угла между валами биссекторной плоскостью (рис. 3). Угол наклона
валов двойных жёстких К. м. может достигать 38°. При углах наклона валов 3-50
применяют упругий К. м. (рис. 4), гибкие элементы к-рого выполняют из
прочного эластичного материала.
Лит.: Мерцалов H. И., Теория пространственных механизмов, M., 1951;
Зиновьев В. А., Пространственные механизмы с низшими парами, М.- Л., 1952;
Артоболевский И. И., Теория машин и механизмов, 2 изд., M., 1967.
E. M. Стариков.
КАРДАНО (Cardano) Джероламо (Иеронимус) [24.9.1501 (по др. данным,
1506), Павия,- 21.9.1576, Рим], итальянский философ, врач и математик.
Разработал космологич. систему ("О тонкости вещей", 1550; "Об
изменчивости вещей", 1557), близкую др. аналогичным построениям натурфилософии
Возрождения (Б. Телезио, Дж. Бруно и др.). При заметных
чертах материализма (вечная материя полагается основою вещей) в ней доминирует
мистич. неоплатонизм. По К., мир строится из трёх элементов - земли, воды,
воздуха; у материи два свойства - теплота и влажность; огонь - только форма
существования всепроницающего и вездесущего небесного тепла, т. е. материи,
сближаемой, т. о., со светом неоплатоников. Становлением вещи обязаны мировой
душе. Ум, единый у всех людей,- пассивен, и лишь божеств, начало, в нём
заложенное, делает возможным богопознание в мистич. восхождении. От ума К.
отличает интеллект, активный элемент человеческого сознания; сущность вещей
человек постигает только там, где объект, как в математике, этой высшей форме
познания, создаётся интеллектом и ему уподобляется. Натурфилософия К.- и
основат. и окончат. синтез его разнообразнейшей учёной деятельности в области
астрологии и алхимии, медицины и физики, математики, инженерии, психологии и т.
д. Работы К. сыграли большую роль в развитии алгебры; одним из первых в Европе
он стал допускать отрицат. корни уравнений. С именем К. связывают формулу
решения неполного кубич. уравнения (Кардано формула). К. занимался
также вопросами передачи движения, теорией рычагов и др. (см. Карданная
передача, Карданный механизм).
Соч.: Opera omnia, v. 1 - 10, Lugdini, 1663; в рус. пер.- О моей жизни, M.,
1938.
Лит.: С т р о и к Д. Я., Краткий очерк истории математики, пер. с
нем., 2 изд., M., 1969; R i v а г i E., La Mente di G. Cardano, Bologna,
1906: S i m i 1 i A., G. Cardano nella luce e nell'ombra del suo tempo, Mil.,
1941; Bellini A., G. Cardano e il suo tempo, Mil., 1947.
H. В. Котрелев.
КАРДАНО ФОРМУЛА, формула для нахождения корней кубического уравнения
x3 + px + q = 0
(к такому виду может быть приведено всякое кубич. уравнение). К. ф. имеет
следующий вид:
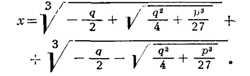
Всякий кубич. корень имеет три значения, среди к-рых не более одного
действительного. Значения кубических корней, стоящих в К. ф., следует брать
такими, чтобы их произведение было равно - р/3; именно эти значения и нужно
складывать, чтобы получить корень уравнения. Таким путём можно найти три корня
уравнения (см. Кубическое уравнение). К. ф. назв. по имени Дж. Кардано
и впервые была опубликована им в 1545, хотя вопрос о том, была она найдена
самим Кардано или заимствована им от H. Тарталъи, или даже ещё раньше
(ок. 1515) открыта С. Ферро, нельзя считать вполне решённым.